Rappel du nombre de liaisons qui doit entourer chaque atome: |
H : 1 C : 4 |
||
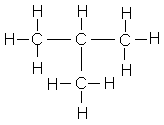
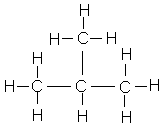
Deuxième solution : |
|||
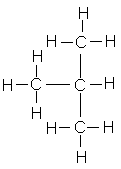
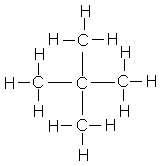
Formule développée de la molécule: |
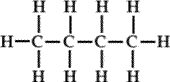 |
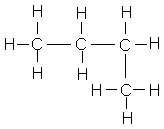
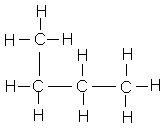
Formule développée de la molécule: |
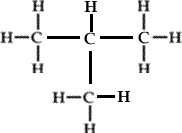 |
Formule semi-développée : |
|
Formule semi-développée : |
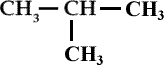 |
Nom : |
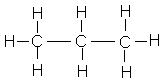
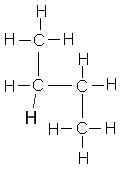
Butane |
Nom : |
2-méthylpropane |